الأمونيا
معرف المنتج
مزود الصين
التعبئة والتغليف برميل
نقاء %99
7664-41-7 CAS No
معلومات الاتصال
الهاتف 2150591759-086+
فاكس 2150591759-086+
البريد الإلكتروني shanghaichemex.anna@gmail.com
anna_chemicaltrader WeChat
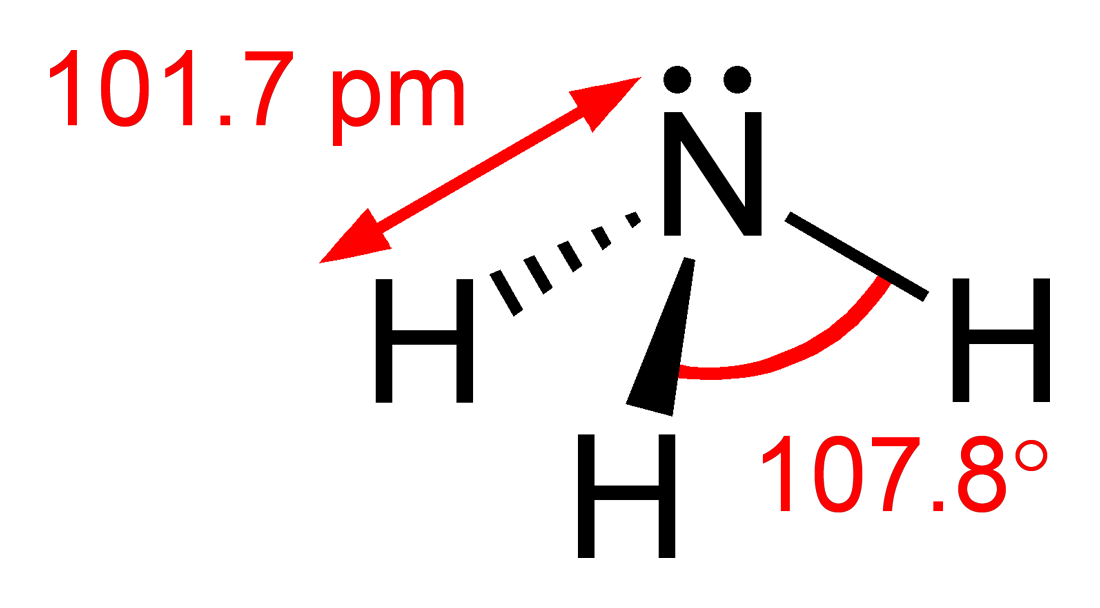
الأمونيا
هو سائل غير عضوي و عديم لون يستخدم في صناعة الأغذية، الصيدلة، الورق و إنتاج المواد الكيميائية الأخرى مثل اليوريا، حمض النيتريك و ما إلی ذلك. الأمونيا هو العنصر الرئيسي في معظم التركیبات النتروجينیة في الصناعة و بالتالي أحد من أهم المواد الرئیسیة غير العضوية. يرتبط تخليق الأمونيا ارتباطاً وثيقاً بإنتاج الأسمدة الصناعية مثل كبريتات الأمونيوم و نترات الأمونيوم و اليوريا و فوسفات الأمونيوم.
المرادفات: نیتریت الهیدروجین، نیترو سیل، ثلاثي هیدروجین النیتریت
1. التطبیقات
من تطبیقات نیترو سیل هي:
- السماد الكیمیائي: يستخدم حوالي 80 ٪ من مجموع الأمونيا لإنتاج الأسمدة النيتروجينية، تشمل هذه الأسمدة كبريتات الأمونيوم، نترات الأمونيوم، فوسفات الأمونيوم و اليوريا.
- صناعة البلاستيك: يتم استخدام حوالي 10 ٪ من الأمونيا لإنتاج البولي يوريثان، راتنجات اليوريا، الفورمالديهايد، النايلون، البولي أكريلونيتريل و … .
- الكيمياء العضوية: هذا المركب مطلوب لتخليق الأميدات، النتريل، و الأمينات.
- الكیمیاویات: تخلیق حمض النيتريك، نيترو غلیسیرين، كربونات هیدروجين الصوديوم، كربونات الصوديوم، سيانيد الهيدروجين و هيدرازين
- المتفجرات: نترات الأمونيوم
- الصيدلية: یستخدم في صنع السلفوناميد و فیتامین B
- الورق: كبريتيد أمونيوم الهيدروجين
- التعدين و Metallurgi: یتم استخدامه في استخراج الزنك و النيكل
یمكن تصنیف تطبیقات هذه المادة بشكل آخر إلی فئتین: الصناعیة و غیر الصناعیة
- التطبیق الصناعي: یستخدم في نظام محفز منخفض لتقليل انبعاثات NOX، صناعة الزراعة، إنتاج حامض النتريك و نترات الأمونيوم، صناعة الألوان، الوقود و مشتقاته، البسكويت (الأمونيا الصالح للأكل) و كعامل مؤكسد و منخفض.
- التطبیق غیر الصناعي: یتم استخدامه في صناعة الأغذية، تكریر المياه، إنتاج المتفجرات، التحكم في تلوث الهواء و التبريد.

2. الإنتاج
ينتج الأمونيا على نطاق واسع بحتة بواسطة الغاز التخليقي أي خليط من النيتروجين و الهيدروجين بنسبة 1:3 على النحو التالي:
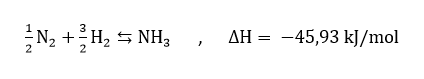
هذا التفاعل يعتمد على أبحاث هابر عام 1904 بناء على التوازن بين النيتروجين و الهيدروجين و الأمونيا. يحدث التفاعل الحراري بين النيتروجين و الهيدروجين في وجود المحفزات المناسبة و سيصاحب الانخفاض في حجم الخلیط. يمكن تحقق أعلى تركيز لنیتریت الهیدروژن في الغاز التخلیقي في أعلى ضغط ممكن و أدنى درجة حرارة ممكنة. يتم تحديد درجة حرارة التفاعل حسب نوع المحفز و نشاطه.
2.1. الأساسیات
جميع مصانع المنتج في العالم تعمل على أساس هذه المبادئ الأساسية، تختلف الوحدات من حيث تصميم المنشآت، تكوين المحفز، معالجة الغاز التخلیقي. الخطوات المهمة في عملية المنتج في المصانع الحديثة بشكل تالي:
- إنتاج خليط من النيتروجين و الهيدروجين كمنتج ثانوي
- إنتاج أول أكسيد الكربون إلى ثاني أكسيد الكربون
- خروج ثاني أكسيد الكربون و (إذا لزم الأمر) كبريتيد الهيدروجين
- التكریر النهائي للغاز التخلیقي
- تفاعل الغازات التخلیقیة و إخراج الأمونيا الذي یتكون من عملية دورية.
- استخدام مجموعة متنوعة من مفاعلات الأمونيا
بشكل أساسي، توجد فئتان من المفاعلات النوویة: المفاعلات الأنبوبية و المفاعلات متعددة المفاعلات (multi-batch)
تنقسم المجموعة الأولى إلى المفاعلات في نفس الاتجاه و في الاتجاه المعاكس و التي تستخدم في إنتاج المركب، و تنقسم المجموعة الثانية إلى مجموعتين: المبرد مع الغاز التبرید و المبرد مع التبادل الحراري.
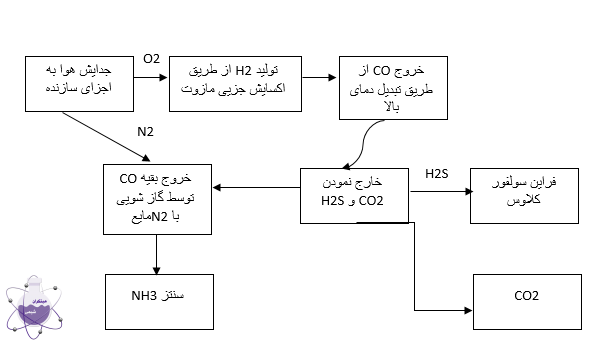
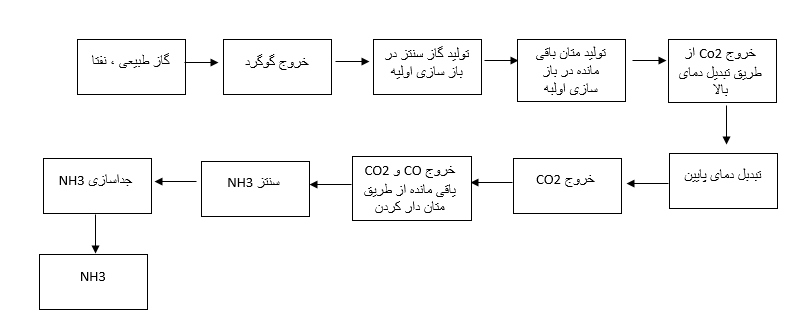
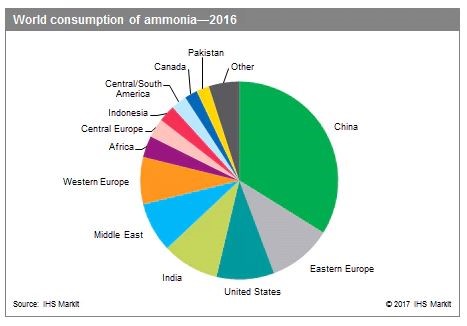
3. السوق العالمیة
كانت القيمة السوقية للأمونيا في عام 2016 حوالي 48.65 مليار دولار، و من المتوقع أن تصل إلى 76.64 مليار دولار حتی عام 2025. سيطرت منطقة آسيا و المحيط الهادئ على هذا السوق في عام 2016، و تتصور التوقعات أسرع نمو في السوق لهذه المنطقة.
4. السلامة
بخار ثلاثي هیدروجین النیترید، و لو كان في التركيز المنخفض، يمكن أن تهيج الجلد و العين و الجهاز التنفسي.
في حالة استنشاق المادة، يجب أن يتعرض المصاب إلى الهواء النقي و يبدأ العلاج فوراً.
في حالة ملامسة العينين، یجب شطفها بكمیة كبیر من الماء لعدة دقائق.
في حالة ملامسة الجلد، يجب شطفه بكمية كبيرة من الماء لمدة 15 دقيقة على الأقل.