حمض الهيدروفلوريك
معرف المنتج
مزود الصين
التعبئة والتغليف برمیل
نقاء %99
7664-39-3 CAS No
معلومات الاتصال
الهاتف 2150591759-086+
فاكس 2150591759-086+
البريد الإلكتروني shanghaichemex.anna@gmail.com
anna_chemicaltrader WeChat
حمض الهيدروفلوريك
مركب كيميائي معدني صيغته الكيميائية هي HF و هو مختلف عن الأحماض الأخرى. هذه المادة في شكلين: دون الماء و قابلة للذوبان في الماء كما أنه عديم اللون و تآكل للغاية.
المرادفات: حمض الفلوریك، فلورید الهیدروجین و HF
كما ذكرنا سابقاً، هذا الحمض شديد التآكل و يمكن للرابطة القوية بين أنيونات الفلوريد و جزيئات السيليكون الزجاجي حل الزجاج فيتم تخزين المركب في حاويات بلاستيكية.
الخصائص الفيزيائية
يتفاعل الهيدروفلوريك مع الزجاج و الفخار و الخرسانة و المطاط و عديد من المعادن، غاز الهيدروجين الذي ينتج بعد التفاعل مع المعادن خطير و متفجر.
لا يمكن تخزين غاز HF في أسطوانات فولاذية لأكثر من عامين بسبب الإمكانات و الضغط الزائد المنتج عن تكوين غاز الهيدروجين. ثابت التوازن لهذه المادة صغير جداً، لذا یذیب فلوريد الهيدروجين جزيئياً و قابل للامتزاج في الماء. الحمض هذا من أحماض الهیدروهیلیك التي ليس لها حموضة قوية.
عندما يتعرض حمض الهيدروفلوريك للهواء یبخر بسرعة و یطلق غازاً رائحته سیئة.
التطبیقات
يتم استخدام فلوريد الهيدروجين بشكل أساسي في الحالات التالیة:
- إنتاج الفلوريد غير العضوية مثل فلوريد الألومنيوم، ثلاثي فلورید البور، رباعي فلوريد اليورانيوم، فلوريد هيدروجين الأمونيوم
- كمادة خام لإنتاج مركبات هامة بما في ذلك الأدوية و البوليمرات مثل تفلون
- إنتاج مركبات الفلور العضوية خاصة الهيدروكربونات الفلورية الهالوجينية
- للحفر و التلميع في صناعة الزجاج
- كمحفز في تفاعلات ألكيلات
- لتخلیل الفولاذ المقاوم للصدأ
- إنتاج أشباح الموصلات
- كمنتج ثانوي لإنتاج حامض الفوسفوريك
- كمادة خام في الصناعات الكیماویة، المعدن، التكرير و لشطف المعادن
طریقة الإنتاج
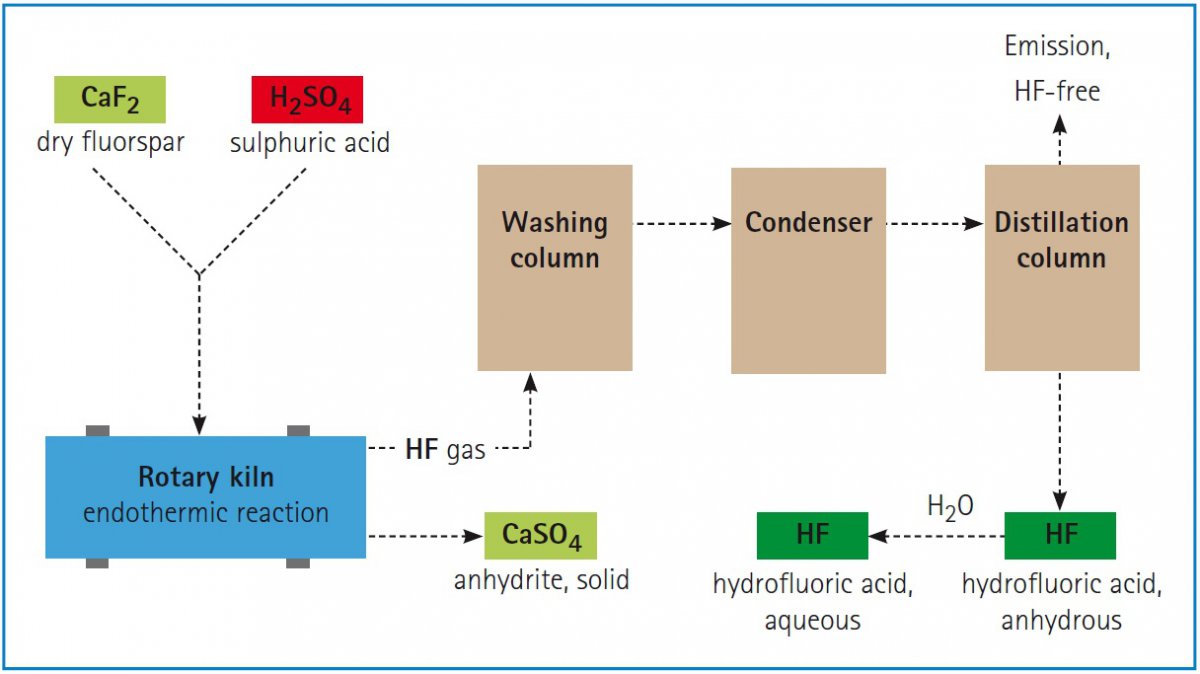
ینتج حمض الهيدروفلوريك أثناء التفاعل بين حمض الكبريتيك المركز و الفلور المعدني (CaF2) في حرارة 250 درجة مئوية و يتم إنتاج فلوريد الهيدروجين و كبريتات الكالسيوم وفقاً للتفاعل التالي:
CaF2 + H2SO4 → 2 HF + CaSO4
خام الفلوريت هو مصدر رئيسي لإنتاج HF العالمي كما أنه يستخدم كمنتج جانبي في إنتاج حمض الفوسفوريك الذي يستخرج من الأباتيت المعدني.
یحتوي الأباتيت عادة على نسبة صغيرة من الفلوراباتيت. بعد فصل المواد الصلبة، تتفاعل الغازات مع حمض الكبريتيك و الزيت و یتم الحصول علی HF دون الماء. بالنظر إلی أن المادة تؤاكل فيرتبط إنتاجها بحل المعادن السيليكات و تنتج كمية كبيرة من حمض الفلوروسيليك.
أهمية اقتصادية
یعتبر حمض الهيدروفلوريك من المنتجات الرئيسية في إنتاج المواد الكيميائية الفلورية. كان استهلاك فلوريد الهيدروجين في الولايات المتحدة حوالي 103*260 طناً عام 1985. وضحت في الجدول التالي طاقة الإنتاج لهذه المادة في أنحاء مختلفة من العالم عام 1986.
| الیابان | آسیا | أسترالیا | أفریقیا | الاتحاد السوفیتي السابق |
| 135 | 150 | 10 | 6 | 100 |
| أوروبا الشرقیة | أوروبا
الغربیة |
المكسیك | كندا | الولایات المتحدة الأمریكیة |
| 140 | 362.5 | 120 | 35 | 306 |
السلامة
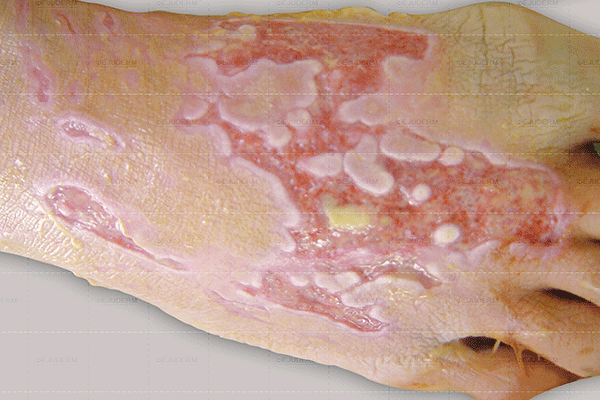
حمض الفلوريك مادة سامة، أيونات الفلور في حمض HF أو بخاره تهاجم على أنسجة الجلد و العظام و تتسبب أضراراً جسيمة و سوف يستمر الأضرار حتى يتم استهلاك كل الأيونات. عند الإتلاف بحامض الفلورايد فلا يشعر بألم و حروق بشكل ملحوظ (لا یظهر الحروق المنتج من هذا الحمض إلا بعد ساعات من ملامسته) لكن الأيونات تتدهور تحت أنسجة الجسم تدهوراً شدیداً و لا ينبغي الإهمال في تشخيصه الأولي. استنشاق غاز HF يمكن أن يضر بالرئتين بشكل دائم. عند ملامسته، يختلف علاجه عن العلاج للأحماض القوية مثل حمض الكبريتيك و حمض الهيدروكلوريك. یمكن HF في تركيز عالي انسداد مجرى الهواء و ذمة رئوية حادة. عندما یلامس الجلد بحمض الفلوریك، ینشأ منطقة حمراء في كثیر من الأحیان لونه أبیض أو رمادي نتيجة لتخثر الأنسجة.
التدابیر اللازمة
- شطف المنطقة على الفور مع كثير من الماء لإزالة HF الزائد علی الجلد
- أخذ الملابس بسرعة و استخدام جل غلوكونات الكالسيوم كل من 15 دقیقة مرة واحدة حتی توقف الألم
- المراجعة إلی الطبیب علی الفور
- الاستفادة من القفازات البلاستیكیة عند ملامسة جلد المصاب
- عدم استخدام المراهم المهدئة أو المراهم المسكنة أبداً
- في حالة ملامسة العينين، یجب غسل العینین بالماء و غلوكونات الكالسيوم لمدة 20 دقيقة.
- في حالة الاستنشاق، یجب تبعید الشخص المصاب من مصدر HF فوراً.
- إذا كان المصاب لا یقدر على التنفس، فیجب التنفس الصناعي علی الفور. (لا تستفد من طریقة الفم إلى الفم في التنفس الصناعي.)







